 © Reuters. 国内第五款CAR-T官宣获批首日即开处方 仍有行业支付难题待解 0291 -1.62% 从投资组合添加/删除 添加至自选组合 添加头寸
© Reuters. 国内第五款CAR-T官宣获批首日即开处方 仍有行业支付难题待解 0291 -1.62% 从投资组合添加/删除 添加至自选组合 添加头寸
头寸已成功添加至:
请给您的持仓投资组合命名 类型: 买入 卖出 日期: 数量: 价格 基点值: 杠杆: 1:1 1:10 1:25 1:50 1:100 1:200 1:400 1:500 1:1000 佣金: 创建新自选组合 创建 创建新持仓投资组合 添加 创建 + 添加其他头寸 结束 600196 +0.77% 从投资组合添加/删除 添加至自选组合 添加头寸
头寸已成功添加至:
请给您的持仓投资组合命名 类型: 买入 卖出 日期: 数量: 价格 基点值: 杠杆: 1:1 1:10 1:25 1:50 1:100 1:200 1:400 1:500 1:1000 佣金: 创建新自选组合 创建 创建新持仓投资组合 添加 创建 + 添加其他头寸 结束 002007 +0.41% 从投资组合添加/删除 添加至自选组合 添加头寸
头寸已成功添加至:
请给您的持仓投资组合命名 类型: 买入 卖出 日期: 数量: 价格 基点值: 杠杆: 1:1 1:10 1:25 1:50 1:100 1:200 1:400 1:500 1:1000 佣金: 创建新自选组合 创建 创建新持仓投资组合 添加 创建 + 添加其他头寸 结束
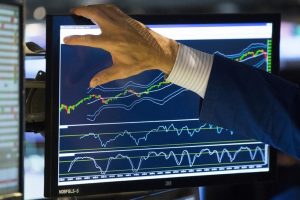
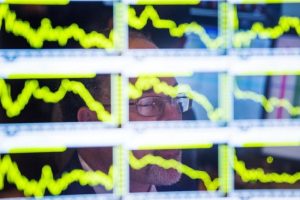
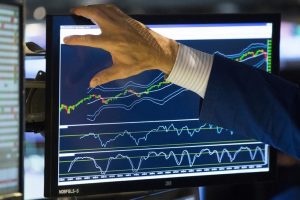
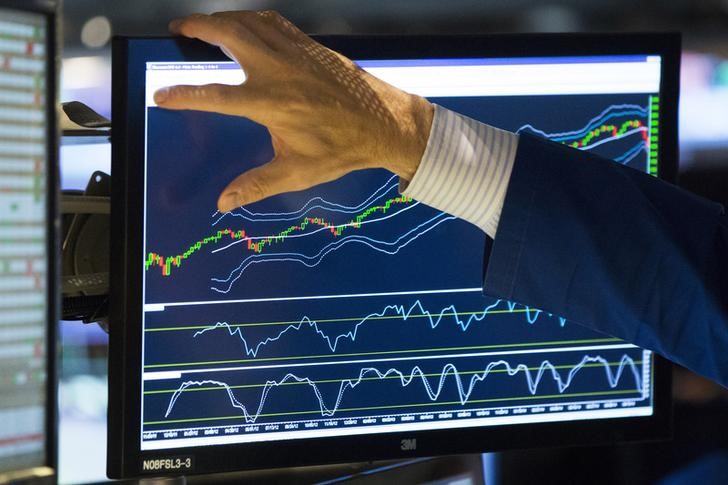
财联社3月2日讯(记者 何凡)今日国内第五款CAR-T疗法——科济药业(02171.HK)治疗多发骨髓瘤新药泽沃基奥仑赛注射液获批上市,并于今日开出全国首张处方。
不过,该药品的上市未给科济药业的股价带来太多的提振作用,公司管线商业化的第一步虽已迈出,但CAR-T疗法昂贵的价格或将限制其可及性的推广,随着越来越多的企业推出创新支付方案,CAR-T疗法未来的商业化道路是否会更加宽广?
国内第五款CAR-T疗法获批
今日午间,科济药业公告,国家药品监督管理局已经正式批准赛恺泽®(泽沃基奥仑赛注射液,产品编号:CT053,一种针对BCMA的自体CAR-T候选产品)的新药上市申请,用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。
据悉,泽沃基奥仑赛注射液的获批是基于一项在中国进行的开放标签、单臂、多中心II期的临床试验(LUMMICAR STUDY 1,NCT03975907)。根据2022年美国血液学会(“ASH”)公布的试验结果,赛恺泽®表现出令人鼓舞的疗效和良好的安全性。
科济药业创始人李宗海博士在微信公众号中表示:“我们期待赛恺泽®能为复发或难治性多发性骨髓瘤成人患者带来更多的希望,改善他们的生存状况。秉承‘科创济世’的愿景,我们将持续探索新技术,拓展拥有全球权益的产品管线,解决CAR-T细胞疗法面临的重大挑战,并为全球癌症患者带来创新和差异化的细胞疗法。”
但今日CT053的上市似乎并未给科济药业的股价带来太多的提振,盘中公司股价一度最高涨逾13%,但市场的热情很快退却,截至收盘,股价下跌0.6%。
值得一提的是,2023年12月12日,科济药业发布公告,称公司在美国子公司CARsgen Therapeutics Corporation于北京时间12月11日晚上收到美国食品药品监管局(FDA)的通知,要求暂停生产CT053、CT041和CT071的临床试验,等待对位于北卡罗来纳州达勒姆的生产基地进行检测后得出的结论。翌日二级市场上,公司股价最大跌幅超33%,截至收盘跌逾30%,收盘价创历史新低。
CAR-T疗法商业化之路漫漫
此次,泽沃基奥仑赛注射液的上市对科济药业来说意义重大,其改变了公司尚无产品上市的情况。
据科济药业提供给财联社记者的资料,今日浙江、北京开出赛恺泽全国首张处方。两名患者均于2021年被诊断为多发性骨髓瘤,并先后接受了诸如诱导治疗、自体造血干细胞移植、免疫加靶向药物等治疗后,仍于2023年再次出现疾病迅速进展或复发情况,浙江省肿瘤医院血液科和解放军总医院第五医学中心血液病医学部淋巴瘤—浆细胞疾病科为患者开出赛恺泽处方。
此外,2023年1月16日,华东医药(000963.SZ)与科济药业宣布就泽沃基奥仑赛注射液达成在中国大陆地区的商业化合作,根据协议条款,华东医药将支付2亿人民币的首付款,以及最高不超过10.25亿人民币的注册及销售里程碑付款。科济药业将继续负责CT053在中国大陆地区的开发、注册和生产。
但由于CAR-T疗法是一种高度个性化的免疫细胞治疗手段,其价格非常昂贵,在中国市场上动辄数百万元一剂的价格往往让人却步。
而在国内,此前NMPA曾批准了4款CAR-T产品,包括,2021年6月获批的复星凯特的奕凯达(阿基仑赛)用于治疗弥漫大B细胞淋巴瘤,120万一针;2021年9月获批药明巨诺-B(02126.HK)的倍诺达(瑞基奥仑赛)用于治疗弥漫大B细胞淋巴瘤,129万一针;2023年6月获批的信达生物/驯鹿医疗的伊基奥仑赛,用于治疗多发性骨髓瘤,116万一针;2023年11月获批的合源生物的纳基奥仑赛,用于治疗B细胞急性淋巴细胞白血病,99.9万一针。
为提高可及性,CAR-T企业曾希望进入国家医保。此前阿基仑赛注射液以及瑞基奥仑赛注射液因出现在2023年国家医保谈判初审名单中引发热议,但最终两款CAR-T疗法均折戟于医保谈判,而这已是CAR-T疗法第三次止步医保谈判。
随着行业赛道越来越拥挤,CAR-T企业正在探索多种创新支付方式。1月11日复星凯特携手宸汐健康宣告,推出奕凯达中国首款淋巴瘤按疗效价值支付计划,原本120万一针的CAR-T治疗,符合条件的患者在使用奕凯达治疗后,若未能达到完全缓解(CR),将获得最高60万元人民币的返还。
此外,药明巨诺方面曾向财联社记者表示,对于高值药品特别是CAR-T治疗,已有产品获批上市的公司都在尝试创新的路径或方式来提升患者的可及性和可负担性,这也算是一种探索。瑞基奥仑赛注射液自上市以来,也陆续推出了创新支付的方案以及升级方案,以协助肿瘤患者提高对CAR-T产品的可及、可负担性。
医药行业资深人士李长城向财联社记者表示,当前CAR-T这类产品的竞争是比较激烈的,推出创新支付方式也是为了应对市场变化。价格上不一定会越来越便宜,但是它会打破一些医疗的治疗方案,很多医疗器械企业和药企可能会推出联合用药,组合治疗方案等。也会引起国家医保局的重视,甚至会参考推出最佳的治疗方案和最优化的治疗价格,CAR-T疗法未来完全有可能进医保,毕竟这和医保目前的政策目的是接近的。
国内第五款CAR-T官宣获批首日即开处方 仍有行业支付难题待解